~ヒト・畜産動物・養殖魚・伴侶動物等の感染症に対する組換えタンパク質ワクチン開発~
感染免疫制御学講座では、ヒト、家畜動物(豚、鶏)、養殖魚(ハタ、ハマチ、サケ等)、伴侶動物(猫)等の感染症に対するワクチンの研究開発を進めています。近年特にウイルス様粒子(VLPs)をワクチンとして完成させる技術開発を進めており、いくつか既にVLP構築に成功しています。また、以前から志賀毒素(Stx)に対するワクチン開発も手がけており、Stxの一種が原因で発症する豚の浮腫病に対するワクチン(スイムジェンSTX)は、2020年12月10日付で農林水産省から認可されました。
このような感染症ワクチンの開発は、当講座単独で進めているのではなく、琉球大学認定スタートアップである株式会社ジェクタス・イノベーターズ(https://jectasinnovators.com/)と二人三脚体制で対応しており、また、国内外の製薬企業(主に動物用医薬品メーカー)との共同研究開発体制の下で進めています。
当講座では主に組換えタンパク質性のサブユニットワクチンに興味をもって開発を進めているため、抗原タンパク質の分子設計(分子改変)を比較的得意としています。病原体が感染拡大するために必須のタンパク質抗原をワクチンの標的分子として選抜し、その構成ドメイン構造などを適切に選抜・改変すると同時に、大腸菌、酵母、昆虫細胞等の発現系を駆使することで、有効性と安全性に優れたワクチン抗原分子を設計します。分子設計(デザイン)に関し、より具体的には、①アミノ酸置換、②タンパク質ドメイン構造置換、③異種タンパク質・ドメイン構造等の足場タンパク質分子への搭載(接木)、あるいは、④これらを組み合わせた独自の分子デザインでワクチン抗原の免疫原性と感染防御能を最大限高めることが当講座の技術的特徴です。
以上のような独自の分子デザインによって、これまで、「豚の浮腫病を予防するワクチン」(志賀毒素)、「鶏の産卵低下症候群(EDS)予防ワクチン」(トリアデノウイルス)、「豚サーコウイルス2型予防ワクチン」などの抗原開発に成功しています。近年では、家畜動物だけでなく、養殖魚を対象とした水産ワクチンや伴侶動物(ペット)用のワクチンの研究開発も進めています。
さらに、感染症診断技術の開発も進めています。主にイムノクロマト法に基づく迅速・簡便診断法の開発です。また、天然物や合成化合物等からワクチンのアジュバントとして機能しうる免疫賦活物質の探索とその免疫学的作用機序を解析する研究も進めています。


株式会社ジェクタス・イノベーターズの会社パンフレット
先述のとおり当講座は、株式会社ジェクタス・イノベーターズと二人三脚体制で基礎から実用化までの研究開発プロセスに関わっていますが、PoC(概念実証)の過程で試作したワクチン抗原などの機能性が確認できた時点で、製造のノウハウについては主に製薬企業に頼るところが大きくなっていきます。
この基礎から製品化までのプロセスは、大きく別けて3通りあります。ひとつ目は、最初から特定の製薬企業のニーズを理解したうえでその製薬企業と一緒に一から研究開発を進める方法です。この場合、特定の製薬企業から研究開発テーマを提示してもらい、その製品等の開発を依頼される形を取ることが多いです。二つ目は、私共の基礎研究成果に基づき、その成果に興味を示した製薬企業と一緒に研究開発を進めていく方法です。三つ目は、製薬企業パートナー無しにほとんどのPoCを我々独自に進めた課題について、製薬企業がライセンスインを求めるような形で対応する方法です。なお、これらの何れの形態を取る場合でも必要に応じて秘密保持契約、共同研究契約、共同特許出願契約等を締結します。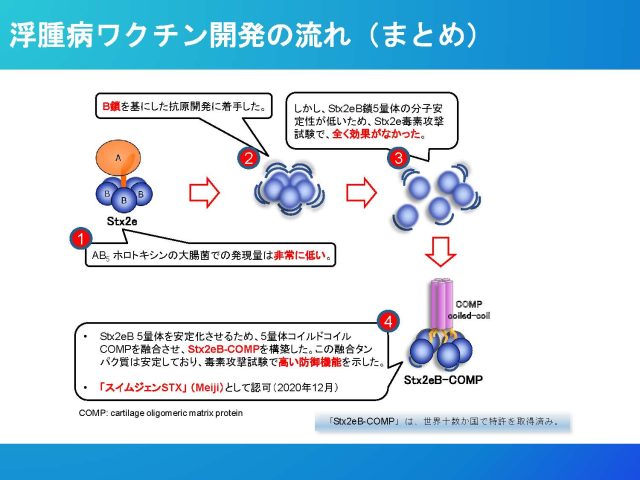
浮腫病ワクチン開発の流れ
特許
- 「ブタサーコウイルス2型VLPワクチン」PCT/JP2020/24491(2020年6月23日)
- 「産卵低下症候群(EDS)予防ワクチン」特許第6620386号(2019年11月29日)
- 「バベシア原虫の表面抗原タンパク質、バベシア原虫に対する抗体の検出方法、バベシア症の診断方法」PCT/JP2019/008255(2019年2月25日)
- 「豚の浮腫病を予防するワクチン」特許第6172585(2017年7月14日):その他、米国、欧州等、世界17の国と地域で特許取得済み
- 「薬物運搬体並びにこれを利用したアジュバントおよびワクチン」特許第5557254号(2014年6月13日)
- 「樹状細胞表面タンパク質に対する抗体を有するバイオナノカプセル」特許第5458286号(2014年1月24日)
- 「ヘテロ型5量体組換えワクチン」特許第4623625号(2010年11月12日)
- 「日本脳炎ワクチンによる西ナイルウイルスの感染に対する交叉防御」特開2003-313140(2003年11月6日)
- 「マラリア原虫伝搬阻止粘膜ワクチン」特開2003-277292(2003年10月2日)
- 「日本脳炎ワクチンをコードする遺伝子を含むトランスジェニック植物」特開2003-116385(2003年4月22日)
- 「免疫寛容の誘導方法」特開2002-085068(2002年3月26日)
論文
- Tsubokawa D, Lee JM, Hatta T, Mikami F, Maruyama H, Arakawa T, Kusakabe T, Tsuji N. (2019) Characterization of the RAGE-binding protein, Strongyloides venestatin, produced by the silkworm-baculovirus expression system. Infection, Genetics and Evolution 75:103964.
- Matsuo H, Somiya M, Iijima M, Arakawa T, Kuroda S. (2018) CD11c-specific bio-nanocapsule enhances vaccine immunogenicity by targeting immune cells. Journal of Nanobiotechnology 16(1):59.
- Harakuni T, Andoh K, Sakamoto R, Tamaki Y, Miyata T, Uefuji H, Yamazaki K, Arakawa T. (2016) Fiber knob domain lacking the shaft sequence but fused to a coiled coil is a candidate subunit vaccine against egg-drop syndrome. Vaccine 34(27):3184.
- Tamaki Y, Harakuni T, Yamaguchi R, Miyata T, Arakawa T. (2016) Cholera toxin B subunit pentamer reassembled from Escherichia coli inclusion bodies for use in vaccination. Vaccine 34(10):1268.
- Fukui M, Shinjo K, Umemura M, Shigeno S, Harakuni T, Arakawa T, Matsuzaki G. (2015) Enhanced effect of BCG vaccine against pulmonary Mycobacterium tuberculosis infection in mice with lung Th17 response to mycobacterial heparin-binding hemagglutinin adhesin antigen. Microbiology and Immunology 59(12):735.


